Difference between revisions of "ब्रोमीन एजाइड"
m (Deepak moved page ब्रोमीन अजाइड to ब्रोमीन एजाइड without leaving a redirect) |
|||
| Line 44: | Line 44: | ||
}} | }} | ||
}} | }} | ||
ब्रोमीन एजाइड | '''ब्रोमीन एजाइड''' एक विस्फोटक अकार्बनिक यौगिक है जिसका सूत्र BrN3 है। इसे कमरे के तापमान पर क्रिस्टल या लाल तरल के रूप में वर्णित किया गया है। यह तापमान और दबाव में छोटे बदलावों के प्रति बेहद संवेदनशील है विस्फोट Δp ≥ 0.05 Torr पर और क्रिस्टलीकरण पर भी होता है इस प्रकार इस रसायन के साथ काम करते समय अत्यधिक सावधानी बरतनी चाहिए। | ||
== तैयारी == | == तैयारी == | ||
ब्रोमिन एजाइड को सोडियम एजाइड की {{chem2|Br2}} के साथ अभिक्रिया द्वारा तैयार किया जा सकता है। इस प्रतिक्रिया से ब्रोमीन एजाइड और सोडियम ब्रोमाइड बनता है : | |||
:{{chem2|NaN3 + Br2 → BrN3 + NaBr}} | :{{chem2|NaN3 + Br2 → BrN3 + NaBr}} | ||
== संरचना == | == संरचना == | ||
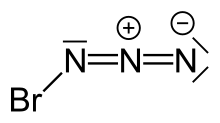
ब्रोमीन एज़ाइड की उच्च संवेदनशीलता के कारण इसकी क्रिस्टल संरचना को समझने में कठिनाई हुई है। इसके | ब्रोमीन एज़ाइड की उच्च संवेदनशीलता के कारण इसकी क्रिस्टल संरचना को समझने में कठिनाई हुई है। इसके अतिरिक्त केंद्रित [[अवरक्त लेजर]] विकिरण के साथ एक लघु [[क्षेत्र-पिघलने]] की प्रक्रिया का उपयोग करके ब्रोमीन एज़ाइड की एक क्रिस्टल संरचना प्राप्त की गई है। आयोडीन एज़ाइड ({{chem2|IN3}}) के विपरीत जो क्रिस्टलीकरण पर एक अंतहीन श्रृंखला जैसी संरचना बनाता है {{chem2|BrN3}} एक पेचदार संरचना बनाता है। प्रत्येक अणु एक ट्रांस-बेंट संरचना को अपनाता है जो गैस चरण में भी पाया जाता है।<ref name="solid">{{cite journal|last=Lyhs|first=Benjamin|author2=Bläser, Dieter|author3=Wölper, Christoph|author4=Schulz, Stephan|author5=Jansen, Georg|date=20 February 2012|title=ब्रोमीन एज़ाइड की ठोस-अवस्था संरचना|journal=Angewandte Chemie International Edition|volume=51|issue=8|pages=1970–1974|doi=10.1002/anie.201108092|pmid=22250068|url=https://nbn-resolving.org/urn:nbn:de:hbz:464-20201112-095746-7 }}</ref> | ||
== प्रतिक्रियाएं == | == प्रतिक्रियाएं == | ||
ब्रोमियम एजाइड | ब्रोमियम एजाइड आयनिक और फ्री-रेडिकल जोड़ के माध्यम से एल्केन्स में जोड़ता है प्रत्येक उत्पादों में एक विपरीत अभिविन्यास देता है। आयनिक योग [[त्रिविम]] विशेष रूप से ट्रांस में होता है।<ref>{{cite journal |last=Liu |first=Robert |title=2,3-Bis(perfluormethyl)bicyclo2.2.2]octa-2,5,7-trienes and their photorearrangement reactions |journal=J. Am. Chem. Soc. |year=1968 |volume=90 |issue=1 |pages=215–216 |doi=10.1021/ja01003a041}}</ref> | ||
ब्रोमीन एज़ाइड से जुड़ी प्रतिक्रियाओं के साथ काम करना मुश्किल है। अणु बहुत प्रतिक्रियाशील है और आसानी से विस्फोट करने के लिए जाना जाता है। यह इसे विस्फोटकों में एक प्रमुख अभिकर्मक बनाता है।<ref>{{cite book |editor1-last=Perry |editor1-first=Dale L. |title=अकार्बनिक यौगिकों की पुस्तिका|year=1995 |publisher=CRC Press |location=Boca Raton |isbn=0-8493-8671-3 |pages=74}}</ref> ब्रोमीन एजाइड के साथ [[प्रकाश रसायन]] के प्रयोगों में पाया गया है कि ब्रोमीन एजाइड के एक छोटे से नमूने के [[यूवी फोटोलिसिस]] के परिणामस्वरूप पूरे नमूने का पृथक्करण हो गया जिससे यह अस्थिर हो गया। एज़ाइड अणुओं के समान नमूनों ने ऐसा प्रभाव नहीं दिखाया। यह ब्रोमीन एज़ाइड की अस्थिर प्रवृत्ति को दर्शाता है कि सूर्य के प्रकाश की उपस्थिति में भी ब्रोमीन एज़ाइड एक प्रतिक्रियाशील अणु होगा।<ref>{{cite journal |last=Henshaw |first=T. L. |author2=David, S. J. |author3=MacDonald, M. A. |author4=Gilbert, J. V. |author5=Stedman, D. H. |author6=Coombe, R. D. |title=ब्रोमीन एज़ाइड का संपार्श्विक अपघटन|journal=J. Phys. Chem. |year=1987 |volume=91 |issue=9 |pages=2287–2293 |doi=10.1021/j100293a016}}</ref> | |||
== सुरक्षा == | == सुरक्षा == | ||
ब्रोमीन एज़ाइड को संभालते समय बहुत सावधानी बरतनी चाहिए क्योंकि यह संभावित रूप से जहरीला होता है और विभिन्न परिस्थितियों में विस्फोट करने में सक्षम होता है। कार्बनिक सॉल्वैंट्स में केंद्रित समाधान भी फट सकते हैं। तरल [[ हरताल ]], [[सोडियम]], [[पर्णिका]] या [[फास्फोरस]] के संपर्क में आने पर फट जाता है। जब अपघटन के लिए गर्म किया जाता है तो यह ब्रोमीन के अत्यधिक जहरीले धुएं का उत्सर्जन करता है और फट जाता है। प्रयोग के दौरान उपयोग किए जाने वाले यौगिक की मात्रा 2 mmol तक सीमित होनी चाहिए। यह रासायनिक प्रतिक्रिया द्वारा वाष्प के रूप में संभावित मध्यम आग का खतरा भी पैदा करता है। यह एक शक्तिशाली ऑक्सीडेंट भी है।<ref name = solid/> | ब्रोमीन एज़ाइड को संभालते समय बहुत सावधानी बरतनी चाहिए क्योंकि यह संभावित रूप से जहरीला होता है और विभिन्न परिस्थितियों में विस्फोट करने में सक्षम होता है। कार्बनिक सॉल्वैंट्स में केंद्रित समाधान भी फट सकते हैं। तरल [[ हरताल |हरताल]], [[सोडियम]], [[पर्णिका]] या [[फास्फोरस]] के संपर्क में आने पर फट जाता है। जब अपघटन के लिए गर्म किया जाता है तो यह ब्रोमीन के अत्यधिक जहरीले धुएं का उत्सर्जन करता है और फट जाता है। प्रयोग के दौरान उपयोग किए जाने वाले यौगिक की मात्रा 2 mmol तक सीमित होनी चाहिए। यह रासायनिक प्रतिक्रिया द्वारा वाष्प के रूप में संभावित मध्यम आग का खतरा भी पैदा करता है। यह एक शक्तिशाली ऑक्सीडेंट भी है।<ref name = solid/> | ||
[[अमेरिकी परिवहन विभाग]] द्वारा इसे [[संयुक्त राज्य अमेरिका]] में परिवहन से प्रतिबंधित कर दिया गया है। | [[अमेरिकी परिवहन विभाग]] द्वारा इसे [[संयुक्त राज्य अमेरिका]] में परिवहन से प्रतिबंधित कर दिया गया है। | ||
Latest revision as of 13:45, 27 May 2023
| |
| Names | |
|---|---|
| IUPAC name
Bromine azide
| |
| Other names
Bromine nitride, Nitrogen bromide, Azidobromide
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
PubChem CID
|
|
| |
| |
| Properties | |
| BrN3 | |
| Molar mass | 121.924 g/mol |
| Appearance | Red liquid |
| Density | N/A |
| Melting point | −45 °C (−49 °F; 228 K) |
| Boiling point | Explodes |
| Structure[1] | |
| tetragonal | |
| I4cd | |
Formula units (Z)
|
16 |
| Hazards | |
| Occupational safety and health (OHS/OSH): | |
Main hazards
|
This is a poison that can spontaneously explode.[2] It explodes on contact with arsenic, sodium, silver foil, or phosphorus. It has a hazard class of 1.1A. |
| Related compounds | |
Related compounds
|
Hydrazoic acid Fluorine azide Chlorine azide Iodine azide |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
ब्रोमीन एजाइड एक विस्फोटक अकार्बनिक यौगिक है जिसका सूत्र BrN3 है। इसे कमरे के तापमान पर क्रिस्टल या लाल तरल के रूप में वर्णित किया गया है। यह तापमान और दबाव में छोटे बदलावों के प्रति बेहद संवेदनशील है विस्फोट Δp ≥ 0.05 Torr पर और क्रिस्टलीकरण पर भी होता है इस प्रकार इस रसायन के साथ काम करते समय अत्यधिक सावधानी बरतनी चाहिए।
तैयारी
ब्रोमिन एजाइड को सोडियम एजाइड की Br2 के साथ अभिक्रिया द्वारा तैयार किया जा सकता है। इस प्रतिक्रिया से ब्रोमीन एजाइड और सोडियम ब्रोमाइड बनता है :
- NaN3 + Br2 → BrN3 + NaBr
संरचना
ब्रोमीन एज़ाइड की उच्च संवेदनशीलता के कारण इसकी क्रिस्टल संरचना को समझने में कठिनाई हुई है। इसके अतिरिक्त केंद्रित अवरक्त लेजर विकिरण के साथ एक लघु क्षेत्र-पिघलने की प्रक्रिया का उपयोग करके ब्रोमीन एज़ाइड की एक क्रिस्टल संरचना प्राप्त की गई है। आयोडीन एज़ाइड (IN3) के विपरीत जो क्रिस्टलीकरण पर एक अंतहीन श्रृंखला जैसी संरचना बनाता है BrN3 एक पेचदार संरचना बनाता है। प्रत्येक अणु एक ट्रांस-बेंट संरचना को अपनाता है जो गैस चरण में भी पाया जाता है।[1]
प्रतिक्रियाएं
ब्रोमियम एजाइड आयनिक और फ्री-रेडिकल जोड़ के माध्यम से एल्केन्स में जोड़ता है प्रत्येक उत्पादों में एक विपरीत अभिविन्यास देता है। आयनिक योग त्रिविम विशेष रूप से ट्रांस में होता है।[3]
ब्रोमीन एज़ाइड से जुड़ी प्रतिक्रियाओं के साथ काम करना मुश्किल है। अणु बहुत प्रतिक्रियाशील है और आसानी से विस्फोट करने के लिए जाना जाता है। यह इसे विस्फोटकों में एक प्रमुख अभिकर्मक बनाता है।[4] ब्रोमीन एजाइड के साथ प्रकाश रसायन के प्रयोगों में पाया गया है कि ब्रोमीन एजाइड के एक छोटे से नमूने के यूवी फोटोलिसिस के परिणामस्वरूप पूरे नमूने का पृथक्करण हो गया जिससे यह अस्थिर हो गया। एज़ाइड अणुओं के समान नमूनों ने ऐसा प्रभाव नहीं दिखाया। यह ब्रोमीन एज़ाइड की अस्थिर प्रवृत्ति को दर्शाता है कि सूर्य के प्रकाश की उपस्थिति में भी ब्रोमीन एज़ाइड एक प्रतिक्रियाशील अणु होगा।[5]
सुरक्षा
ब्रोमीन एज़ाइड को संभालते समय बहुत सावधानी बरतनी चाहिए क्योंकि यह संभावित रूप से जहरीला होता है और विभिन्न परिस्थितियों में विस्फोट करने में सक्षम होता है। कार्बनिक सॉल्वैंट्स में केंद्रित समाधान भी फट सकते हैं। तरल हरताल, सोडियम, पर्णिका या फास्फोरस के संपर्क में आने पर फट जाता है। जब अपघटन के लिए गर्म किया जाता है तो यह ब्रोमीन के अत्यधिक जहरीले धुएं का उत्सर्जन करता है और फट जाता है। प्रयोग के दौरान उपयोग किए जाने वाले यौगिक की मात्रा 2 mmol तक सीमित होनी चाहिए। यह रासायनिक प्रतिक्रिया द्वारा वाष्प के रूप में संभावित मध्यम आग का खतरा भी पैदा करता है। यह एक शक्तिशाली ऑक्सीडेंट भी है।[1]
अमेरिकी परिवहन विभाग द्वारा इसे संयुक्त राज्य अमेरिका में परिवहन से प्रतिबंधित कर दिया गया है।
संदर्भ
- ↑ 1.0 1.1 1.2 Lyhs, Benjamin; Bläser, Dieter; Wölper, Christoph; Schulz, Stephan; Jansen, Georg (20 February 2012). "ब्रोमीन एज़ाइड की ठोस-अवस्था संरचना". Angewandte Chemie International Edition. 51 (8): 1970–1974. doi:10.1002/anie.201108092. PMID 22250068.
- ↑ Patnaik, Pradyot (2007). A Comprehensive Guide to the Hazardous Properties of Chemical Substances. 615: Wiley-Interscience. p. 615. ISBN 978-0-471-71458-3.
{{cite book}}: CS1 maint: location (link) - ↑ Liu, Robert (1968). "2,3-Bis(perfluormethyl)bicyclo2.2.2]octa-2,5,7-trienes and their photorearrangement reactions". J. Am. Chem. Soc. 90 (1): 215–216. doi:10.1021/ja01003a041.
- ↑ Perry, Dale L., ed. (1995). अकार्बनिक यौगिकों की पुस्तिका. Boca Raton: CRC Press. p. 74. ISBN 0-8493-8671-3.
- ↑ Henshaw, T. L.; David, S. J.; MacDonald, M. A.; Gilbert, J. V.; Stedman, D. H.; Coombe, R. D. (1987). "ब्रोमीन एज़ाइड का संपार्श्विक अपघटन". J. Phys. Chem. 91 (9): 2287–2293. doi:10.1021/j100293a016.
- Chemical articles with multiple compound IDs
- Multiple chemicals in an infobox that need indexing
- Articles without EBI source
- Articles without KEGG source
- Articles without UNII source
- Pages using collapsible list with both background and text-align in titlestyle
- Articles containing unverified chemical infoboxes
- Templates that generate short descriptions
- Collapse templates
- Navigational boxes
- Navigational boxes without horizontal lists
- Sidebars with styles needing conversion
- Templates generating microformats
- Templates that are not mobile friendly
- Wikipedia metatemplates
- ब्रोमीन (I) यौगिक
- एज़िडो यौगिक
- विस्फोटक रसायन
- स्यूडोहैलोजन
- Machine Translated Page
- Created On 19/05/2023