ट्राइमेथिलगैलियम

| |
| |
| Names | |
|---|---|
| IUPAC name
trimethylgallane, trimethanidogallium
| |
| Identifiers | |
3D model (JSmol)
|
|
| ChemSpider | |
PubChem CID
|
|
| |
| |
| Properties | |
| Ga(CH3)3 | |
| Molar mass | 114.827 g/mol |
| Appearance | colourless liquid |
| Melting point | −15 °C (5 °F; 258 K) |
| Boiling point | 55.7 °C (132.3 °F; 328.8 K) |
| Reacts with water | |
| Hazards | |
| Occupational safety and health (OHS/OSH): | |
Main hazards
|
Pyrophoric (can ignite spontaneously in air), reacts with water to release methane |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
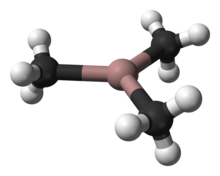
ट्राइमेथिलगैलियम, जिसे अक्सर टीएमजी या टीएमजीए के रूप में संक्षिप्त किया जाता है, गा (सीएच) सूत्र वाला ऑर्गेनोगैलियम यौगिक है।3)3. यह एक रंगहीन, ज्वरनाशक द्रव है।[1] ट्राइमिथाइलएल्यूमिनियम के विपरीत, टीएमजी एक मोनोमेरिक संरचना को अपनाता है।[2] जब विस्तार से जांच की गई, तो मोनोमेरिक इकाइयाँ स्पष्ट रूप से कई कमजोर Ga---C इंटरैक्शन से जुड़ी हुई हैं, जो ट्राइमेथिलिण्डियम की स्थिति की याद दिलाती हैं।[3]
तैयारी
टीएमजी के दो रूपों की आम तौर पर जांच की जाती है: लुईस बेस एडक्ट्स या टीएमजी। सभी विभिन्न मिथाइलेटिंग एजेंटों के साथ गैलियम ट्राइक्लोराइड की प्रतिक्रियाओं द्वारा तैयार किए जाते हैं। जब दिएथील ईथर में मिथाइलमैग्नेशियम आयोडाइड के साथ मिथाइलेशन किया जाता है, तो उत्पाद में खराब वाष्पशील डायथाइल ईथर एडक्ट उत्पन्न होता है। ईथर लिगैंड आसानी से नष्ट नहीं होता है, हालांकि इसे तरल अमोनिया के साथ विस्थापित किया जा सकता है।[4] जब तृतीयक फॉस्फीन की उपस्थिति में मिथाइल लिथियम के साथ एल्किलेशन किया जाता है तो वायु-स्थिर फॉस्फीन एडक्ट प्राप्त होता है:
- GaCl3 + 3 MeLi + PR3 → R3P−GaMe3 + 3 LiCl
ठोस फॉस्फीन योजक को वैक्यूम के तहत गर्म करने से आधार-मुक्त टीएमजी मुक्त हो जाता है:[1]:R3P−GaMe3 → R3P + GaMe3 अन्य गैर-वाष्पशील आधारों का वर्णन किया गया है।[5] टीएमजी के संश्लेषण के लिए अन्य मिथाइलेटिंग एजेंटों में डाइमिथाइलजिंक और ट्राइमिथाइलएल्यूमिनियम शामिल हैं।
अनुप्रयोग
टीएमजी गैलियम युक्त यौगिक अर्धचालकों, जैसे गैलियम आर्सेनाइड, गैलियम नाइट्राइड, गैलियम फॉस्फाइड, गैलियम एंटीमोनाइड, इंडियम गैलियम आर्सेनाइड, इंडियम गैलियम नाइट्राइड, एल्यूमीनियम गैलियम इंडियम फॉस्फाइड, के मेटलऑर्गेनिक वाष्प चरण एपिटैक्सी (एमओवीपीई) के लिए गैलियम का पसंदीदा धातुकार्बनिक स्रोत है। इंडियम गैलियम फॉस्फाइड, AlInGaNP और गैलियम ऑक्साइड|गा2O3.[6] इन सामग्रियों का उपयोग एलईडी प्रकाश व्यवस्था और अर्धचालकों के उत्पादन में धातुकार्बनिक रासायनिक वाष्प जमाव अग्रदूत के रूप में किया जाता है।
संदर्भ
- ↑ 1.0 1.1 Bradley, D. C.; Chudzynska, H. C.; Harding, I. S. (1997). "ट्राइमिथाइलिंडियम और ट्राइमिथाइलगैलियम". Inorganic Syntheses. 31: 67–74. doi:10.1002/9780470132623.ch8. ISBN 9780470132623.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ Mitzel, Norbert W.; Lustig, Christian; Berger, Raphael J. F.; Runeberg, Nino (2002). "ट्राइमेथाइल- और ट्राइथाइलगैलियम की ल्यूमिनेसेंस घटना और ठोस-अवस्था संरचनाएं". Angewandte Chemie International Edition. 41 (14): 2519–2522. doi:10.1002/1521-3773(20020715)41:14<2519::AID-ANIE2519>3.0.CO;2-2.
- ↑ Kraus, C. A.; Toonder, F. E. (1933). "ट्राइमिथाइल गैलियम, ट्राइमिथाइल गैलियम ईथरेट और ट्राइमिथाइल गैलियम अमाइन". PNAS. 19 (3): 292–8. Bibcode:1933PNAS...19..292K. doi:10.1073/pnas.19.3.292. PMC 1085965. PMID 16577510.
- ↑ Foster, Douglas F.; Cole-Hamilton, David J. (1997). "Electronic Grade Alkyls of Group 12 and 13 Elements". Inorganic Syntheses. 31: 29-66. doi:10.1002/9780470132623.ch7.
- ↑ Shenai-Khatkhate, D. V.; Goyette, R. J.; Dicarlo, R. L. Jr; Dripps, G. (2004). "यौगिक अर्धचालकों के MOVPE विकास में उपयोग किए जाने वाले स्रोतों के लिए पर्यावरण, स्वास्थ्य और सुरक्षा के मुद्दे". Journal of Crystal Growth. 272 (1–4): 816–21. Bibcode:2004JCrGr.272..816S. doi:10.1016/j.jcrysgro.2004.09.007.
- Articles without EBI source
- Articles without KEGG source
- Articles without UNII source
- Pages using collapsible list with both background and text-align in titlestyle
- Articles containing unverified chemical infoboxes
- Templates that generate short descriptions
- Collapse templates
- Navigational boxes
- Navigational boxes without horizontal lists
- Sidebars with styles needing conversion
- Templates generating microformats
- Templates that are not mobile friendly
- Wikipedia metatemplates
- रासायनिक वाष्प जमाव अग्रदूत
- गैलियम यौगिक
- मिथाइल कॉम्प्लेक्स
- पायरोफोरिक सामग्री
- Machine Translated Page
- Created On 14/12/2023