नाइट्रट करना
कार्बनिक रसायन विज्ञान में, नाइट्रो समूह की शुरूआत के लिए नाइट्रेशन रासायनिक प्रक्रियाओं का एक सामान्य वर्ग है (−NO2) एक कार्बनिक यौगिक में। यह शब्द नाइट्रेट एस्टर बनाने की विभिन्न प्रक्रियाओं के लिए भी गलत तरीके से लागू होता है (−ONO2) अल्कोहल (रसायन विज्ञान) और नाइट्रिक एसिड के बीच (जैसा कि नाइट्रोग्लिसरीन के कार्बनिक संश्लेषण में होता है)। नाइट्रो यौगिकों और नाइट्रेट्स के परिणामी आणविक संरचनाओं के बीच का अंतर (NO−3) यह है कि नाइट्रो यौगिकों में नाइट्रोजन परमाणु एक गैर-ऑक्सीजन परमाणु (आमतौर पर कार्बन या अन्य नाइट्रोजन परमाणु) के लिए सीधे रासायनिक बंधन होता है, जबकि नाइट्रेट एस्टर (जिन्हें कार्बनिक नाइट्रेट भी कहा जाता है) में, नाइट्रोजन एक ऑक्सीजन परमाणु से जुड़ा होता है। बारी आमतौर पर एक कार्बन परमाणु (नाइट्रिटो समूह) से बंधी होती है।
सख्त अर्थों में नाइट्रेशन के कई प्रमुख औद्योगिक अनुप्रयोग हैं; मात्रा के हिसाब से सबसे महत्वपूर्ण nitrobenzene जैसे नाइट्रोएरोमैटिक यौगिकों के उत्पादन के लिए हैं। विस्फोटकों के उत्पादन के लिए विशेष रूप से नाइट्रेशन प्रतिक्रियाओं का उपयोग किया जाता है, उदाहरण के लिए गुआनिडीन को नाइट्रोगुआनाइडिन में बदलना और टोल्यूनि को ट्रिनिट्रोटोलुइन (टीएनटी) में बदलना। हालांकि, प्रतिक्रिया मध्यवर्ती और प्रीकर्सर (रसायन विज्ञान) के रूप में उनका व्यापक महत्व है। सालाना लाखों टन नाइट्रोएरोमैटिक्स का उत्पादन होता है।[1]
सुगंधित नाइट्रेशन
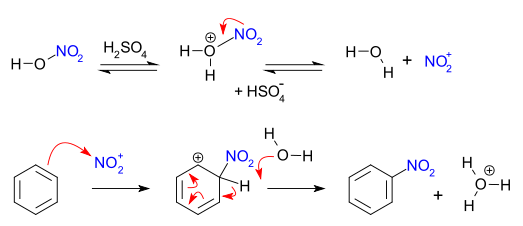
विशिष्ट नाइट्रेशन संश्लेषण तथाकथित मिश्रित एसिड, केंद्रित नाइट्रिक एसिड और सल्फ्यूरिक एसिड का मिश्रण लागू करते हैं।[2] यह मिश्रण नाइट्रोनियम आयन (NO2+), जो सुगंधित नाइट्रेशन में सक्रिय प्रजाति है। यह सक्रिय संघटक, जिसे नाइट्रोनियम टेट्राफ्लोरोबोरेट के मामले में पृथक किया जा सकता है,[3] मिश्रित एसिड की आवश्यकता के बिना भी नाइट्रेशन को प्रभावित करता है। मिश्रित-एसिड संश्लेषण में सल्फ्यूरिक एसिड का सेवन नहीं किया जाता है और इसलिए उत्प्रेरक के साथ-साथ पानी के लिए एक अवशोषक के रूप में कार्य करता है। बेंजीन के नाइट्रेशन के मामले में, प्रतिक्रिया गर्म तापमान पर आयोजित की जाती है, जो 50 डिग्री सेल्सियस से अधिक नहीं होती है। [4] प्रक्रिया इलेक्ट्रोफिलिक सुगन्धित प्रतिस्थापन का एक उदाहरण है, जिसमें इलेक्ट्रॉन-समृद्ध बेंजीन रिंग द्वारा हमला शामिल है:
एसिटाइल नाइट्रेट का उपयोग नाइट्रेशन एजेंट के रूप में भी किया गया था।[7][8]
स्कोप
चयनात्मकता नाइट्रेशन में एक चुनौती हो सकती है क्योंकि एक नियम के रूप में एक से अधिक यौगिक परिणाम हो सकते हैं लेकिन केवल एक ही वांछित है, इसलिए वैकल्पिक उत्पाद संदूषक के रूप में कार्य करते हैं या बस बर्बाद हो जाते हैं। तदनुसार, उपयुक्त चयनात्मकता के साथ संश्लेषण डिजाइन करना वांछनीय है; उदाहरण के लिए, प्रतिक्रिया की स्थिति को नियंत्रित करके, फ्लोरोनोन को चुनिंदा ट्रिनिट्रेट किया जा सकता है[9] या टेट्रानाइट्रेटेड।[10] सुगन्धित छल्लों पर प्रतिस्थापन इस इलेक्ट्रोफिलिक सुगन्धित प्रतिस्थापन की प्रतिक्रिया दर को प्रभावित करते हैं। अन्य नाइट्रो यौगिक समूहों जैसे निष्क्रिय करने वाले समूहों में इलेक्ट्रॉन-निकासी प्रभाव होता है। ऐसे समूह प्रतिक्रिया को निष्क्रिय (धीमा) करते हैं और सुगंधित मेटा स्थिति पर हमला करने के लिए इलेक्ट्रोफिलिक नाइट्रोनियम आयन को निर्देशित करते हैं। निष्क्रिय करने वाले मेटा-निर्देशन प्रतिस्थापनों में सल्फोनील, साइनो समूह, कीटोन, एस्टर और कार्बोक्सिलेट्स शामिल हैं। एमिनो , हाइड्रॉकसिल और मिथाइल समूहों जैसे सक्रिय समूहों द्वारा नाइट्रेशन को तेज किया जा सकता है और पैरा और ऑर्थो आइसोमर्स के परिणामस्वरूप एमाइड और ईथर भी हो सकते हैं।
एक स्रोत के अनुसार नाइट्रिक एसिड और सल्फ्यूरिक एसिड के साथ रंगों का रासायनिक आधार का सीधा नाइट्रेशन,[11] परिणाम पैरा- और मेटा-नाइट्रोएनिलिन आइसोमर्स के 50/50 मिश्रण में होता है। इस प्रतिक्रिया में तेजी से प्रतिक्रिया करने वाला और सक्रिय करने वाला एनिलिन (ArNH2) अधिक प्रचुर मात्रा में लेकिन कम प्रतिक्रियाशील (निष्क्रिय) एनिलिनियम आयन (ArNH) के साथ संतुलन में मौजूद है3+), जो इस प्रतिक्रिया उत्पाद वितरण की व्याख्या कर सकता है। एक अन्य सूत्र के अनुसार,[12] एनिलिन का अधिक नियंत्रित नाइट्रेशन एसिटिक एनहाईड्राइड के साथ अभिक्रिया द्वारा एसीटैनिल्स का के निर्माण के साथ शुरू होता है जिसके बाद वास्तविक नाइट्रेशन होता है। क्योंकि एमाइड एक नियमित सक्रिय समूह है, जो उत्पाद बनते हैं वे पैरा और ऑर्थो आइसोमर्स हैं। प्रतिक्रिया मिश्रण को गर्म करना एमाइड को नाइट्रेटेड एनिलिन में वापस हाइड्रोलाइज करने के लिए पर्याप्त है।
वोल्फेंस्टीन-बोटर्स प्रतिक्रिया में, बेंजीन नाइट्रिक एसिड और मरकरी (II) नाइट्रेट के साथ प्रतिक्रिया करके पिरक अम्ल देता है।
इप्सो नाइट्रेशन
एरील क्लोराइड्स, ट्राइफलेट्स और नॉनफ्लेट्स के साथ, एरीन प्रतिस्थापन पैटर्न#Ipso.2C meso.2C और पेरी प्रतिस्थापन नाइट्रेशन भी हो सकता है।[13] इप्सो नाइट्रेशन वाक्यांश का पहली बार उपयोग पेरिन और स्किनर द्वारा 1971 में क्लोरोएनिसोल नाइट्रेशन की जांच में किया गया था।[14] एक प्रोटोकॉल में, 4-क्लोरो-एन-ब्यूटिलबेंज़ीन को सोडियम नाइट्राइट के साथ tert-butanol|t-butanol में 0.5 mol% Tris(dibenzylideneacetone)dipalladium(0)|Pd की उपस्थिति में प्रतिक्रिया दी जाती है2(डीबीए)3, 4-नाइट्रो-एन-ब्यूटिलबेंजीन प्रदान करने के लिए एक बायरिल्फोस्फीन लिगैंड और एक चरण-स्थानांतरण उत्प्रेरक।[15]
यह भी देखें
- मेनके नाइट्रेशन
- जिंक नाइट्रेशन
- प्रतिक्रियाशील नाइट्रोजन प्रजातियां
संदर्भ
- ↑ Gerald Booth (2007). "नाइट्रो यौगिक, सुगंधित". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_411. ISBN 978-3527306732.
- ↑ John McMurry Organic Chemistry 2nd Ed.
- ↑ George A. Olah and Stephen J. Kuhn. "Benzonitrile, 2-methyl-3,5-dinitro-". Organic Syntheses.; Collective Volume, vol. 5, p. 480
- ↑ "Nitration of benzene and methylbenzene".
- ↑ Esteves, P. M.; Carneiro, J. W. M.; Cardoso, S. P.; Barbosa, A. G. H.; Laali, K. K.; Rasul, G.; Prakash, G. K. S.; e Olah, G. A. (2003). "Unified Mechanism Concept of Electrophilic Aromatic Nitration Revisited: Convergence of Computational Results and Experimental Data". J. Am. Chem. Soc. 125 (16): 4836–49. doi:10.1021/ja021307w. PMID 12696903.
- ↑ Queiroz, J. F.; Carneiro, J. W. M.; Sabino A. A.; Sparapan, R.; Eberlin, M. N.; Esteves, P. M. (2006). "Electrophilic Aromatic Nitration: Understanding Its Mechanism and Substituent Effects". J. Org. Chem. 71 (16): 6192–203. doi:10.1021/jo0609475. PMID 16872205.
- ↑ Bordwell, F. G.; Garbisch, Edgar W. (July 1960). "एसिटाइल नाइट्रेट के साथ नाइट्रेशन। I. नाइट्रेटिंग एजेंट की प्रकृति और सरल अल्केन्स के साथ प्रतिक्रिया का तंत्र". Journal of the American Chemical Society. 82 (14): 3588–3598. doi:10.1021/ja01499a029.
- ↑ Louw, Robert (15 April 2001). "एसिटाइल नाइट्रेट". Encyclopedia of Reagents for Organic Synthesis: ra032. doi:10.1002/047084289X.ra032.
- ↑ E. O. Woolfolk and Milton Orchin. "2,4,7-Trinitrofluorenone". Organic Syntheses.; Collective Volume, vol. 3, p. 837
- ↑ Melvin S. Newman and H. Boden. "2,4,5,7-Tetranitrofluorenone". Organic Syntheses.; Collective Volume, vol. 5, p. 1029
- ↑ Web resource: warren-wilson.edu
- ↑ Mechanism and synthesis Peter Taylor, Royal Society of Chemistry (Great Britain), Open University
- ↑ Prakash, G.; Mathew, T. (2010). "एरेनेस का इप्सो-नाइट्रेशन". Angewandte Chemie International Edition in English. 49 (10): 1726–1728. doi:10.1002/anie.200906940. PMID 20146295.
- ↑ Perrin, C. L.; Skinner, G. A. (1971). "इलेक्ट्रोफिलिक सुगंधित प्रतिस्थापन ("आईपीएसओ कारक") में निर्देशक प्रभाव। हेलोनिसोल का नाइट्रेशन". Journal of the American Chemical Society. 93 (14): 3389. doi:10.1021/ja00743a015.
- ↑ Fors, B.; Buchwald, S. (2009). "पीडी-उत्प्रेरित आर्यल क्लोराइड्स, ट्राइफलेट्स और नॉनफ्लैट्स का नाइट्रोएरोमैटिक्स में रूपांतरण". Journal of the American Chemical Society. 131 (36): 12898–12899. doi:10.1021/ja905768k. PMC 2773681. PMID 19737014.
- Templates that generate short descriptions
- Collapse templates
- Navigational boxes
- Navigational boxes without horizontal lists
- Sidebars with styles needing conversion
- Templates generating microformats
- Templates that are not mobile friendly
- Wikipedia metatemplates
- Navbox orphans
- Organic chemistry navigational boxes
- नाइट्रेशन प्रतिक्रियाएं
- प्रतिस्थापन प्रतिक्रियाएं
- Machine Translated Page
- Created On 11/04/2023