Difference between revisions of "फ़ाँसफ़ोरस तथा अंय तत्त्वों का यौगिक"
m (added Category:Vigyan Ready using HotCat) |
|||
| (9 intermediate revisions by one other user not shown) | |||
| Line 1: | Line 1: | ||
रसायन विज्ञान में, एक फॉस्फाइड एक यौगिक होता है जिसमें P3− आयन या इसके समतुल्य | रसायन विज्ञान में, एक फॉस्फाइड एक यौगिक होता है जिसमें P3− आयन या इसके समतुल्य आयन होते है। व्यापक रूप से भिन्न संरचनाओं के साथ कई अलग-अलग फॉस्फाइड ज्ञात हैं।<ref>{{Greenwood&Earnshaw}}</ref> सामान्यतः बाइनरी फॉस्फाइड्स पर सामना किया जाता है, अर्थात उन सामग्रियों में केवल फास्फोरस और एक कम विद्युतीय तत्व होते हैं। कई पॉलीफॉस्फाइड होते हैं, जो ठोस होते हैं जिनमें आयनिक श्रृंखला या फॉस्फोरस के क्लस्टर होते हैं। फॉस्फाइड को [[पारा (तत्व)]], सीसा, [[सुरमा]], [[विस्मुट]], [[टेल्यूरियम]] और [[ एक विशेष तत्त्व जिस का प्रभाव रेडियो पर पड़ता है | एक विशेष तत्त्व जिस का प्रभाव रेडियो पर पड़ता है]] के अपवाद के साथ अधिकांशता कम विद्युतीय तत्वों के साथ पहचान जाता है।<ref name = "Schnering">Von Schnering, H.G. and Hönle , W. (1994) "Phosphides - Solid-state Chemistry" in ''Encyclopedia of Inorganic Chemistry''. R. Bruce King (ed.). John Wiley & Sons {{ISBN|0-471-93620-0}}</ref> अंत में, कुछ फॉस्फाइड आणविक होते हैं। | ||
== बाइनरी फॉस्फाइड == | == बाइनरी फॉस्फाइड == | ||
बाइनरी फॉस्फाइड में फास्फोरस और एक अन्य तत्व सम्मलित हैं। समूह 1 फॉस्फाइड का एक उदाहरण [[ सोडियम फास्फाइड |सोडियम फास्फाइड]] ({{chem2|Na3P}}) है। अन्य उल्लेखनीय उदाहरणों में [[एल्यूमीनियम फास्फाइड]] ({{chem2|एआईपी}}) और [[कैल्शियम फास्फाइड]] ({{chem2|Ca3P2}}) सम्मलित हैं, जो कीटनाशकों के रूप में उपयोग किए जाते हैं, हाइड्रोलिसिस पर | बाइनरी फॉस्फाइड में फास्फोरस और एक अन्य तत्व सम्मलित होते हैं। समूह 1 फॉस्फाइड का एक उदाहरण [[ सोडियम फास्फाइड |सोडियम फास्फाइड]] ({{chem2|Na3P}}) है। अन्य उल्लेखनीय उदाहरणों में [[एल्यूमीनियम फास्फाइड]] ({{chem2|एआईपी}}) और [[कैल्शियम फास्फाइड]] ({{chem2|Ca3P2}}) सम्मलित हैं, जो कीटनाशकों के रूप में उपयोग किए जाते हैं, हाइड्रोलिसिस पर विषाक्त [[फॉस्फीन]] को छोड़ने की उनकी प्रवृत्ति का शोषण करते हैं। मैग्नीशियम फास्फाइड ({{chem2|Mg3P2}}) भी नमी के प्रति संवेदनशील होते है। [[इंडियम फास्फाइड]] ({{chem2|आईएनपी}}) और [[गैलियम फास्फाइड]] ({{chem2|जीएपी}}) अर्ध-चालकों के रूप में उपयोग किया जाता है, अधिकांशतः संबंधित [[आर्सेनाइड]] के संयोजन में।<ref>{{Cite journal|last1=Blackman|first1=C. S.|last2=Carmalt|first2=C. J.|author-link2=Claire J. Carmalt|last3=O'Neill|first3=S. A.|last4=Parkin|first4=I. P.|last5=Molloy|first5=K. C.|last6=Apostolico|first6=L.|year=2003|title=समूह Vb मेटल फॉस्फाइड पतली फिल्मों का रासायनिक वाष्प जमाव|url=http://discovery.ucl.ac.uk/143120/1/Blackman_Group_VB_2_Corrected.pdf|journal=Journal of Materials Chemistry|volume=13|issue=8|pages=1930|doi=10.1039/b304084b}}</ref> [[कॉपर फास्फाइड]] ({{chem2|Cu3P}}) फॉस्फाइड के लिए एक दुर्लभ स्टोइकोमेट्री दिखाता है। ये यौगिक सभी सॉल्वैंट्स में अघुलनशील हैं - ये 3-आयामी ठोस अवस्था पॉलिमर हैं। इलेक्ट्रोपोसिटिव धातुओं के लिए, सामग्री हाइड्रोलाइज़ होती है: | ||
:{{chem2|Ca3P2 + 6 H2O → 3 Ca(OH)2 + 2 PH3}} | :{{chem2|Ca3P2 + 6 H2O → 3 Ca(OH)2 + 2 PH3}} | ||
== पॉलीफॉस्फाइड्स == | == पॉलीफॉस्फाइड्स == | ||
पॉलीफॉस्फाइड | पॉलीफॉस्फाइड में {{chem2|P\sP}} बंधन होता हैं। सबसे सरल पॉलीफॉस्फाइड में होता है {{chem|P|2|4-}} आयन; अन्य में क्लस्टर सम्मलित है {{chem|P|11|3-}} आयन और बहुलक श्रृंखला वाले आयन (जैसे पेचदार {{chem|(|P|-|)|''n''}} आयन) और जटिल शीट या 3-डी आयन।<ref>{{Cite journal | doi = 10.1080/03086648708080608| title = संक्रमण धातुओं के फॉस्फाइड और पॉलीफॉस्फाइड| journal = Phosphorus and Sulfur and the Related Elements| volume = 30| issue = 1–2| pages = 413–416| year = 1987| last1 = Jeitschko | first1 = W. | last2 = Möller | first2 = M. H. }}</ref> संरचनाओं की सीमा व्यापक है। [[ पोटैशियम ]] में नौ फॉस्फाइड होते हैं: {{chem2|K3P}}, {{chem2|K4P3}}, {{chem2|K5P4}}, {{chem2|KP}}, {{chem2|K4P6}}, {{chem2|K3P7}}, {{chem2|K3P11}}, {{chem2|KP10.3}}, {{chem2|KP15}}. [[निकल]]न के आठ मोनो- और पॉलीफॉस्फाइड भी उपस्थित हैं: ({{chem2|Ni3P}}, {{chem2|Ni5P2}}, {{chem2|Ni12P5}}, {{chem2|Ni2P}}, {{chem2|Ni5P4}}, {{chem2|NiP}}, {{chem2|NiP2}}, {{chem2|NiP3}}).<ref name = "Schnering"/> | ||
दो पॉलीफॉस्फाइड आयन, {{chem|P|3|4-}} पाया गया {{chem|K|4|P|3}} में और {{chem|P|4|5-}} पाया गया {{chem2|K5P4}} में, और विषम संख्या वाले [[ रासायनिक संयोजन इलेक्ट्रॉन |रासायनिक संयोजन इलेक्ट्रॉनो]] के साथ [[कट्टरपंथी आयन]] हैं जो दोनों यौगिकों को अनुचुंबकीय बनाते हैं।<ref name = "Schnering"/> | दो पॉलीफॉस्फाइड आयन, {{chem|P|3|4-}} पाया गया {{chem|K|4|P|3}} में और {{chem|P|4|5-}} पाया गया {{chem2|K5P4}} में, और विषम संख्या वाले [[ रासायनिक संयोजन इलेक्ट्रॉन |रासायनिक संयोजन इलेक्ट्रॉनो]] के साथ [[कट्टरपंथी आयन|रेडिकल आयन]] हैं जो दोनों यौगिकों को अनुचुंबकीय बनाते हैं।<ref name = "Schnering"/> | ||
== फास्फाइड और पॉलीफॉस्फाइड सामग्री की तैयारी == | == फास्फाइड और पॉलीफॉस्फाइड सामग्री की तैयारी == | ||
फॉस्फाइड यौगिक | फॉस्फाइड यौगिक बनाने के कई उपाय हैं। एक सामान्य उपाय में एक धातु और [[लाल फास्फोरस]] (पी) को निष्क्रिय वायुमंडलीय परिस्थितियों या वैक्यूम के तहत गर्म करना सम्मलित है। सिद्धांत रूप में, सभी धातु फॉस्फाइड और पॉलीफॉस्फाइड को मौलिक फास्फोरस और संबंधित धातु तत्व से स्टोइकोमेट्रिक रूपों में संश्लेषित किया जा सकता है। चूंकि, कई समस्याओं के कारण संश्लेषण जटिल है। स्थानीय अति ताप के कारण एक्सोथर्मिक प्रतिक्रियाएं अधिकांशतः विस्फोटक होती हैं। ऑक्सीकृत धातु, या यहां तक कि धातु के बाहरी भाग पर सिर्फ एक ऑक्सीकृत परत, फास्फोरिनेशन शुरू करने के लिए अत्यधिक और अस्वीकार्य रूप से उच्च तापमान का कारण बनती है।<ref>{{cite journal | last1 = von Schnering |first1 = Hans-Georg | last2 = Hönle | first2=Wolfgang | title = फास्फाइड के साथ खाई को पाटना| journal = Chemical Reviews | year = 1988 | volume = 88 | pages = 243–273 | doi = 10.1021/cr00083a012}}</ref> निकल फास्फाइड उत्पन्न करने के लिए हाइड्रोथर्मल प्रतिक्रियाओं ने शुद्ध और अच्छी तरह से क्रिस्टलीकृत निकल फास्फाइड यौगिकों {{chem2|Ni2P}} और {{chem2|Ni12P5}} का उत्पादन किया है। इन यौगिकों को क्रमश: 24 और 48 घंटों के लिए 200 डिग्री सेल्सियस पर {{chem2|NiCl2*12H2O}} और लाल फास्फोरस के बीच एक ठोस-तरल प्रतिक्रिया के माध्यम से संश्लेषित किया गया था।<ref>{{cite journal | author1 = Liu, Zongyi | author2 = Huang, Xiang | author3 = Zhu, Zhibin | author4 = Dai, Jinhui | title = निकेल फॉस्फाइड पाउडर के संश्लेषण के लिए एक सरल हल्का हाइड्रोथर्मल मार्ग| journal = Ceramics International | volume = 36 | year = 2010 | pages = 1155–1158 | doi = 10.1016/j.ceramint.2009.12.015 | issue = 3}}</ref> | ||
मेटल हैलाइड्स के साथ [[ट्रिस (ट्राइमिथाइलसिलिल) फॉस्फीन]] की प्रतिक्रिया से मेटल फॉस्फाइड भी उत्पन्न होते हैं। इस विधि में, हैलाइड को वाष्पशील [[ट्राइमिथाइलसिलिल क्लोराइड]] के रूप में मुक्त किया जाता है। | मेटल हैलाइड्स के साथ [[ट्रिस (ट्राइमिथाइलसिलिल) फॉस्फीन]] की प्रतिक्रिया से मेटल फॉस्फाइड भी उत्पन्न होते हैं। इस विधि में, हैलाइड को वाष्पशील [[ट्राइमिथाइलसिलिल क्लोराइड]] के रूप में मुक्त किया जाता है। | ||
| Line 22: | Line 22: | ||
== प्राकृतिक उदाहरण == | == प्राकृतिक उदाहरण == | ||
कुछ | कुछ मेटोरिते में खनिज [[लेखक साइट|श्राइबर्साइट]] {{chem2|(Fe,Ni)3P}} सामान्य है। | ||
==संदर्भ== | ==संदर्भ== | ||
| Line 34: | Line 34: | ||
[[Category: Machine Translated Page]] | [[Category: Machine Translated Page]] | ||
[[Category:Created On 18/05/2023]] | [[Category:Created On 18/05/2023]] | ||
[[Category:Vigyan Ready]] | |||
Latest revision as of 10:50, 2 June 2023
रसायन विज्ञान में, एक फॉस्फाइड एक यौगिक होता है जिसमें P3− आयन या इसके समतुल्य आयन होते है। व्यापक रूप से भिन्न संरचनाओं के साथ कई अलग-अलग फॉस्फाइड ज्ञात हैं।[1] सामान्यतः बाइनरी फॉस्फाइड्स पर सामना किया जाता है, अर्थात उन सामग्रियों में केवल फास्फोरस और एक कम विद्युतीय तत्व होते हैं। कई पॉलीफॉस्फाइड होते हैं, जो ठोस होते हैं जिनमें आयनिक श्रृंखला या फॉस्फोरस के क्लस्टर होते हैं। फॉस्फाइड को पारा (तत्व), सीसा, सुरमा, विस्मुट, टेल्यूरियम और एक विशेष तत्त्व जिस का प्रभाव रेडियो पर पड़ता है के अपवाद के साथ अधिकांशता कम विद्युतीय तत्वों के साथ पहचान जाता है।[2] अंत में, कुछ फॉस्फाइड आणविक होते हैं।
बाइनरी फॉस्फाइड
बाइनरी फॉस्फाइड में फास्फोरस और एक अन्य तत्व सम्मलित होते हैं। समूह 1 फॉस्फाइड का एक उदाहरण सोडियम फास्फाइड (Na3P) है। अन्य उल्लेखनीय उदाहरणों में एल्यूमीनियम फास्फाइड (एआईपी) और कैल्शियम फास्फाइड (Ca3P2) सम्मलित हैं, जो कीटनाशकों के रूप में उपयोग किए जाते हैं, हाइड्रोलिसिस पर विषाक्त फॉस्फीन को छोड़ने की उनकी प्रवृत्ति का शोषण करते हैं। मैग्नीशियम फास्फाइड (Mg3P2) भी नमी के प्रति संवेदनशील होते है। इंडियम फास्फाइड (आईएनपी) और गैलियम फास्फाइड (जीएपी) अर्ध-चालकों के रूप में उपयोग किया जाता है, अधिकांशतः संबंधित आर्सेनाइड के संयोजन में।[3] कॉपर फास्फाइड (Cu3P) फॉस्फाइड के लिए एक दुर्लभ स्टोइकोमेट्री दिखाता है। ये यौगिक सभी सॉल्वैंट्स में अघुलनशील हैं - ये 3-आयामी ठोस अवस्था पॉलिमर हैं। इलेक्ट्रोपोसिटिव धातुओं के लिए, सामग्री हाइड्रोलाइज़ होती है:
- Ca3P2 + 6 H2O → 3 Ca(OH)2 + 2 PH3
पॉलीफॉस्फाइड्स
पॉलीफॉस्फाइड में P−P बंधन होता हैं। सबसे सरल पॉलीफॉस्फाइड में होता है P4−
2 आयन; अन्य में क्लस्टर सम्मलित है P3−
11 आयन और बहुलक श्रृंखला वाले आयन (जैसे पेचदार (P−
)
n आयन) और जटिल शीट या 3-डी आयन।[4] संरचनाओं की सीमा व्यापक है। पोटैशियम में नौ फॉस्फाइड होते हैं: K3P, K4P3, K5P4, KP, K4P6, K3P7, K3P11, KP10.3, KP15. निकलन के आठ मोनो- और पॉलीफॉस्फाइड भी उपस्थित हैं: (Ni3P, Ni5P2, Ni12P5, Ni2P, Ni5P4, NiP, NiP2, NiP3).[2]
दो पॉलीफॉस्फाइड आयन, P4−
3 पाया गया K
4P
3 में और P5−
4 पाया गया K5P4 में, और विषम संख्या वाले रासायनिक संयोजन इलेक्ट्रॉनो के साथ रेडिकल आयन हैं जो दोनों यौगिकों को अनुचुंबकीय बनाते हैं।[2]
फास्फाइड और पॉलीफॉस्फाइड सामग्री की तैयारी
फॉस्फाइड यौगिक बनाने के कई उपाय हैं। एक सामान्य उपाय में एक धातु और लाल फास्फोरस (पी) को निष्क्रिय वायुमंडलीय परिस्थितियों या वैक्यूम के तहत गर्म करना सम्मलित है। सिद्धांत रूप में, सभी धातु फॉस्फाइड और पॉलीफॉस्फाइड को मौलिक फास्फोरस और संबंधित धातु तत्व से स्टोइकोमेट्रिक रूपों में संश्लेषित किया जा सकता है। चूंकि, कई समस्याओं के कारण संश्लेषण जटिल है। स्थानीय अति ताप के कारण एक्सोथर्मिक प्रतिक्रियाएं अधिकांशतः विस्फोटक होती हैं। ऑक्सीकृत धातु, या यहां तक कि धातु के बाहरी भाग पर सिर्फ एक ऑक्सीकृत परत, फास्फोरिनेशन शुरू करने के लिए अत्यधिक और अस्वीकार्य रूप से उच्च तापमान का कारण बनती है।[5] निकल फास्फाइड उत्पन्न करने के लिए हाइड्रोथर्मल प्रतिक्रियाओं ने शुद्ध और अच्छी तरह से क्रिस्टलीकृत निकल फास्फाइड यौगिकों Ni2P और Ni12P5 का उत्पादन किया है। इन यौगिकों को क्रमश: 24 और 48 घंटों के लिए 200 डिग्री सेल्सियस पर NiCl2·12H2O और लाल फास्फोरस के बीच एक ठोस-तरल प्रतिक्रिया के माध्यम से संश्लेषित किया गया था।[6]
मेटल हैलाइड्स के साथ ट्रिस (ट्राइमिथाइलसिलिल) फॉस्फीन की प्रतिक्रिया से मेटल फॉस्फाइड भी उत्पन्न होते हैं। इस विधि में, हैलाइड को वाष्पशील ट्राइमिथाइलसिलिल क्लोराइड के रूप में मुक्त किया जाता है।
K2P16 लाल फॉस्फोरस और पोटेशियम एथोक्साइड से तैयार करने की एक विधि बताई गई है।[7]
आणविक फॉस्फाइड्स
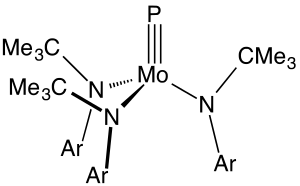
धातु और फास्फोरस के बीच त्रिबंध वाले यौगिक दुर्लभ हैं। मुख्य उदाहरणों में सूत्र है Mo(P)(NR2)3, जहाँ R एक भारी कार्बनिक पदार्थ है।[8]
ऑर्गेनिक फॉस्फाइड्स
कई ऑर्गनोफॉस्फेट ज्ञात हैं। सामान्य उदाहरणों में सूत्र R2PM है जहाँ R एक कार्बनिक पदार्थ है और M एक धातु है। एक उदाहरण लिथियम डाइफेनिलफॉस्फाइड है। ज़िंटल क्लस्टर P3−
7 विविध क्षार धातु व्युत्पन्न के साथ प्राप्त किया जाता है।
प्राकृतिक उदाहरण
कुछ मेटोरिते में खनिज श्राइबर्साइट (Fe,Ni)3P सामान्य है।
संदर्भ
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ 2.0 2.1 2.2 Von Schnering, H.G. and Hönle , W. (1994) "Phosphides - Solid-state Chemistry" in Encyclopedia of Inorganic Chemistry. R. Bruce King (ed.). John Wiley & Sons ISBN 0-471-93620-0
- ↑ Blackman, C. S.; Carmalt, C. J.; O'Neill, S. A.; Parkin, I. P.; Molloy, K. C.; Apostolico, L. (2003). "समूह Vb मेटल फॉस्फाइड पतली फिल्मों का रासायनिक वाष्प जमाव" (PDF). Journal of Materials Chemistry. 13 (8): 1930. doi:10.1039/b304084b.
- ↑ Jeitschko, W.; Möller, M. H. (1987). "संक्रमण धातुओं के फॉस्फाइड और पॉलीफॉस्फाइड". Phosphorus and Sulfur and the Related Elements. 30 (1–2): 413–416. doi:10.1080/03086648708080608.
- ↑ von Schnering, Hans-Georg; Hönle, Wolfgang (1988). "फास्फाइड के साथ खाई को पाटना". Chemical Reviews. 88: 243–273. doi:10.1021/cr00083a012.
- ↑ Liu, Zongyi; Huang, Xiang; Zhu, Zhibin; Dai, Jinhui (2010). "निकेल फॉस्फाइड पाउडर के संश्लेषण के लिए एक सरल हल्का हाइड्रोथर्मल मार्ग". Ceramics International. 36 (3): 1155–1158. doi:10.1016/j.ceramint.2009.12.015.
- ↑ Dragulescu-Andrasi, Alina; Miller, L. Zane; Chen, Banghao; McQuade, D. Tyler; Shatruk, Michael (March 14, 2016). "पोटेशियम एथोक्साइड के साथ प्रतिक्रिया द्वारा घुलनशील पॉलीफॉस्फाइड आयनों में लाल फास्फोरस का सुगम रूपांतरण". Angewandte Chemie International Edition. 55 (12): 3904–3908. doi:10.1002/anie.201511186. PMID 26928980.
- ↑ Cossairt, B. M.; Piro, N. A.; Cummins, C. C. (2010). "प्रारंभिक-संक्रमण-धातु-मध्यस्थ सक्रियण और सफेद फास्फोरस का परिवर्तन". Chemical Reviews. 110 (7): 4164–77. CiteSeerX 10.1.1.666.8019. doi:10.1021/cr9003709. PMID 20175534.
- Collapse templates
- Navigational boxes
- Navigational boxes without horizontal lists
- Sidebars with styles needing conversion
- Templates generating microformats
- Templates that are not mobile friendly
- Wikipedia metatemplates
- आयनों
- फास्फाइड
- फास्फोरस (−III) यौगिक
- Machine Translated Page
- Created On 18/05/2023
- Vigyan Ready