बोरियम
| Bohrium | ||||||
|---|---|---|---|---|---|---|
| उच्चारण | /ˈbɔːriəm/ ( | |||||
| जन अंक | [270] (unconfirmed: 278) | |||||
| Bohrium in the periodic table | ||||||
| ||||||
| Atomic number (Z) | 107 | |||||
| समूह | group 7 | |||||
| अवधि | period 7 | |||||
| ब्लॉक | d-block | |||||
| ऋणावेशित सूक्ष्म अणु का विन्यास | [Rn] 5f14 6d5 7s2[1][2] | |||||
| प्रति शेल इलेक्ट्रॉन | 2, 8, 18, 32, 32, 13, 2 | |||||
| भौतिक गुण | ||||||
| Phase at STP | solid (predicted)[3] | |||||
| Density (near r.t.) | 26–27 g/cm3 (predicted)[4][5] | |||||
| परमाणु गुण | ||||||
| ऑक्सीकरण राज्य | (+3), (+4), (+5), +7[2][6] (parenthesized: prediction) | |||||
| Ionization energies | ||||||
| परमाणु का आधा घेरा | empirical: 128 pm (predicted)[2] | |||||
| सहसंयोजक त्रिज्या | 141 pm (estimated)[7] | |||||
| अन्य गुण | ||||||
| प्राकृतिक घटना | synthetic | |||||
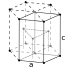
| क्रिस्टल की संरचना | hexagonal close-packed (hcp) (predicted)[3] | |||||
| CAS नंबर | 54037-14-8 | |||||
| History | ||||||
| नामी | after Niels Bohr | |||||
| खोज] | Gesellschaft für Schwerionenforschung (1981) | |||||
| ||||||
बोहरियम रासायनिक प्रतीक Bh और परमाणु संख्या 107 के साथ सिंथेटिक तत्व रासायनिक तत्व है। इसका नाम डेनिश भौतिक विज्ञानी नील्स बोह्र के नाम पर रखा गया है। सिंथेटिक तत्व के रूप में, इसे प्रयोगशाला में बनाया जा सकता है किन्तु यह प्रकृति में नहीं पाया जाता है। बोहरियम के सभी ज्ञात समस्थानिक अत्यधिक रेडियोधर्मी क्षय हैं; सबसे स्थिर ज्ञात आइसोटोप है इस प्रकार 270 बीएच लगभग 2.4 मिनट के आधे जीवन के साथ, चूँकि अपुष्ट 278Bh का आधा जीवन लगभग 11.5 मिनट हो सकता है।
आवर्त सारणी में, यह ब्लॉक (आवर्त सारणी) या डी-ब्लॉक सुपरहेवी तत्व है। यह अवधि 7 तत्व का सदस्य है और संक्रमण धातुओं की 6d श्रृंखला के पांचवें सदस्य के रूप में समूह 7 तत्व से संबंधित है। रसायन विज्ञान के प्रयोगों ने पुष्टि की है कि बोहरियम समूह 7 में रेनीयाम के लिए भारी होमोलॉजी (रसायन विज्ञान) के रूप में व्यवहार करता है। बोहरियम की रासायनिक संपत्ति को केवल आंशिक रूप से चित्रित किया जाता है, किन्तु वे अन्य समूह 7 तत्वों के रसायन विज्ञान के साथ अच्छी तरह से तुलना करते हैं।
परिचय
Introduction to the heaviest elements
सबसे भारी परमाणु नाभिक परमाणु प्रतिक्रियाओं में बनाए जाते हैं जो असमान आकार के दो अन्य नाभिकों को जोड़ते हैं सामान्यतः, द्रव्यमान के संदर्भ में दोनों नाभिक जितने अधिक असमान होते है, दोनों के बीच प्रतिक्रिया होने की संभावना उतनी ही अधिक होती हैं। भारी नाभिक से बनी पदार्थ को एक लक्ष्य में बनाया जाता है, जिस पर हल्के नाभिक की किरण द्वारा बमबारी की जाती है। दो नाभिक एक में तभी मिल सकते हैं जब वे एक-दूसरे के अधिक निकट आएँ थे ; सामान्यतः, नाभिक (सभी धनावेशित) इलेक्ट्रोस्टैटिक प्रतिकर्षण के कारण एक दूसरे को प्रतिकर्षित करते हैं। सशक्त अंतःक्रिया इस प्रतिकर्षण को दूर कर सकती है किन्तु केवल नाभिक से बहुत कम दूरी के अन्दर; इस प्रकार बीम नाभिक के वेग की तुलना में इस तरह के प्रतिकर्षण को महत्वहीन बनाने के लिए बीम नाभिक को बहुत तेज किया जाता है। [19] दो नाभिकों के संलयन के लिए अकेले पास आना पर्याप्त नहीं है: जब दो नाभिक एक-दूसरे के पास आते हैं, जिससे वे सामान्यतः लगभग 10−20 सेकंड तक एक साथ रहते हैं और फिर अलग हो जाते हैं (जरूरी नहीं कि प्रतिक्रिया से पहले उसी संरचना में हों) अतिरिक्त एक एकल बनाने के नाभिक.[19][20] यदि संलयन होता है, जिससे अस्थायी विलय - जिसे यौगिक नाभिक कहा जाता है एक उत्तेजित अवस्था है। जिससे अपनी उत्तेजना ऊर्जा को खोने और अधिक स्थिर स्थिति तक पहुंचने के लिए, एक यौगिक नाभिक या तो विखंडन करता है या एक या कई न्यूट्रॉन को बाहर निकालता है, जो ऊर्जा को दूर ले जाते हैं। यह प्रारंभिक टक्कर के बाद लगभग 10−16 सेकंड में घटित होता है।
इतिहास

आविष्कार
दो समूहों ने रासायनिक तत्व खोजों की समयरेखा को प्रमाणित किया था। बोहरियम के साक्ष्य पहली बार 1976 में यूरी ओगेनेसियन है जिसके नेतृत्व में सोवियत अनुसंधान दल द्वारा सूची किए गए थे, जिसमें बिस्मथ-209 और लेड-208 के लक्ष्य क्रमशः क्रोमियम-54 और मैंगनीज-55 के त्वरित नाभिक के साथ बमबारी किए गए थे।[8] दो गतिविधियाँ देखी गईं, जिससे दो मिलीसेकंड के आधे जीवन के साथ, और दूसरी लगभग पाँच सेकंड के आधे जीवन के साथ प्रोयोग किया गया था। चूंकि इन दोनों गतिविधियों की तीव्रता का अनुपात प्रयोग के समय स्थिर था, यह प्रस्तावित किया गया था कि पहला आइसोटोप बोहरियम-261 से था और दूसरा उसकी बेटी डबनियम -257 से था। इसके पश्चात्, डब्नियम आइसोटोप को डब्नियम-258 में सुधारा गया था, जो वास्तव में पांच सेकंड का आधा जीवन है (ड्यूबनियम-257 का सेकंड का आधा जीवन है); चूँकि, अपने माता-पिता के लिए मनाया गया आधा जीवन बाद में 1981 में डार्मस्टाट में बोहरियम की निश्चित खोज में देखे गए आधे जीवन की तुलना में बहुत कम है। शुद्ध और व्यावहारिक रसायन के अंतर्राष्ट्रीय संघ / आईयूपीएपी ट्रांसफरमियम वर्किंग ग्रुप (टीडब्ल्यूजी) ने निष्कर्ष निकाला कि जबकि डब्नियम-258 शायद इस प्रयोग में देखा गया था, इसके मूल बोहरियम-262 के उत्पादन के प्रमाण पर्याप्त रूप से आश्वस्त नहीं थे।[9]
1981 में, डार्मस्टैड में भारी आयन अनुसंधान के लिए जीएसआई हेल्महोल्ट्ज केंद्र (जीएसआई हेल्महोल्त्ज़जेंट्रम फर श्वेरियोनएनफोर्सचुंग) में पीटर आर्मब्रस्टर और गॉटफ्रीड मुन्ज़ेनबर्ग के नेतृत्व में जर्मन शोध दल ने क्रोमियम-54 के त्वरित नाभिक के साथ बिस्मथ-209 के लक्ष्य पर बमबारी की थी, जिससे 5 परमाणुओं आइसोटोप बोहरियम-262 का उत्पादन हुआ था :[10]
इस खोज को आगे चलकर फेर्मियम और कलिफ़ोरनियम के ज्ञात समस्थानिकों के लिए उत्पादित बोहरियम परमाणुओं की अल्फा क्षय श्रृंखला के उनके विस्तृत माप द्वारा प्रमाणित किया गया था। इंटरनेशनल यूनियन ऑफ प्योर एंड एप्लाइड केमिस्ट्री/आईयूपीएपी ट्रांसफरमियम वर्किंग ग्रुप (टीडब्ल्यूजी) ने अपनी 1992 की सूची में आधिकारिक खोजकर्ताओं के रूप में जीएसआई सहयोग को मान्यता दी थी।[9]
प्रस्तावित नाम
सितंबर 1992 में, जर्मन समूह ने डेनिश भौतिक विज्ञानी नील्स बोह्र के सम्मान में प्रतीक एनएस के साथ नील्सबोरियम नाम का सुझाव दिया था। अप्रैल, रूस में परमाणु अनुसंधान के लिए संयुक्त संस्थान के सोवियत वैज्ञानिकों ने सुझाव दिया था कि यह नाम तत्व 105 (जिसे अंततः डब्नियम कहा जाता है) को दिया जाए और जर्मन टीम बोह्र और इस तथ्य दोनों को पहचानना चाहती थी कि डबना टीम पहली थी ठंड संलयन प्रतिक्रिया का प्रस्ताव करने के लिए, और साथ ही तत्व 105 के नामकरण की विवादास्पद समस्या को हल करने में सहायता करता है। डबना टीम तत्व 107 के लिए जर्मन समूह के नामकरण प्रस्ताव से सहमत है।[11]
एक तत्व नामकरण विवाद था कि 104 से 106 तक के तत्वों को क्या कहा जाना था; आईयूपीएसी ने इस तत्व के लिए अस्थायी, व्यवस्थित तत्व नाम के रूप में नलसेप्टियम प्रतीक Uns को अपनाया था।1994 में आईयूपीएसी की समिति ने पक्षसमर्थन की थी कि तत्व 107 को बोहरियम नाम दिया जाए, नील्सबोरियम नहीं, क्योंकि किसी तत्व के नामकरण में किसी वैज्ञानिक के पूर्ण नाम का उपयोग करने की कोई मिसाल नहीं थी।[12] खोजकर्ताओं द्वारा इसका विरोध किया गया था क्योंकि कुछ चिंता थी कि नाम बोरॉन के साथ भ्रमित हो सकता है और विशेष रूप से उनके संबंधित ऑक्सीजन, बोहराट और बोरेट के नामों की पहचान होती है।इस स्थिति आईयूपीएसी की डेनिश शाखा को दे दिया गया था, जिसने इसके अतिरिक्त, बोहरियम नाम के पक्ष में मतदान किया था,oxyanions और इस प्रकार तत्व 107 के लिए बोहरियम नाम को 1997 में अंतरराष्ट्रीय स्तर पर मान्यता दी गई थी; बोरॉन और बोहरियम के संबंधित ऑक्सीजनों के नाम उनकी समरूपता के अतिरिक्त अपरिवर्तित रहते हैं।[13]
समस्थानिक
| समस्थानिक | अर्ध-जीवन [14][15] |
क्षय | खोज
वर्ष |
प्रतिक्रिया |
|---|---|---|---|---|
| 260Bh | 35 ms | α | 2007 | 209Bi(52Cr,n)[16] |
| 261Bh | 11.8 ms | α | 1986 | 209Bi(54Cr,2n)[17] |
| 262Bh | 84 ms | α | 1981 | 209Bi(54Cr,n)[10] |
| 262mBh | 9.6 ms | α | 1981 | 209Bi(54Cr,n)[10] |
| 264Bh | 0.97 s | α | 1994 | 272Rg(—,2α)[18] |
| 265Bh | 0.9 s | α | 2004 | 243Am(26Mg,4n)[19] |
| 266Bh | 0.9 s | α | 2000 | 249Bk(22Ne,5n)[20] |
| 267Bh | 17 s | α | 2000 | 249Bk(22Ne,4n)[20] |
| 270Bh | 2.4 min[21] | α | 2006 | 282Nh(—,3α)[22] |
| 271Bh | 2.9 s[21] | α | 2003 | 287Mc(—,4α)[22] |
| 272Bh | 8.8 s[21] | α | 2005 | 288Mc(—,4α)[22] |
| 274Bh | 40 s | α | 2009 | 294Ts(—,5α) |
| 278Bh | 11.5 min? | SF | 1998? | 290Fl(e−,νe3α)? |
बोहरियम में कोई स्थिर या प्राकृतिक रूप से पाए जाने वाले समस्थानिक नहीं होते हैं। कई रेडियोधर्मी समस्थानिकों को प्रयोगशाला में संश्लेषित किया गया है, या तो दो परमाणुओं को जोड़कर या भारी तत्वों के क्षय को देखकर बोहरियम के बारह अलग-अलग समस्थानिकों को 260-262, 264-267, 270-272, 274, और 278 परमाणु द्रव्यमान के साथ सूची किया गया है, जिनमें से एक, बोहरियम -262, ज्ञात मेटास्टेबल स्थिति है। ये सभी किन्तु अपुष्ट हैं 278Bh क्षय केवल अल्फा क्षय के माध्यम से होता है, चूँकि कुछ अज्ञात बोहरियम समस्थानिकों के सहज विखंडन से निकलने की पूर्वानुमान की जाती है।[14]
हल्के समस्थानिकों का आधा जीवन सामान्यतः छोटा होता है; 260Bh, 261Bh, 262Bh और 262mBh के लिए 100 एमएस से कम का आधा जीवन देखा गया था। 264Bh, 265Bh, 266Bh, और 271Bh लगभग 1 s पर अधिक स्थिर हैं, और 267Bh और 272Bh का आधा जीवन लगभग 10 सेकंड है। सबसे भारी आइसोटोप सबसे अधिक स्थिर होते हैं, 270Bh और 274Bh का आधा जीवन क्रमशः लगभग 2.4 मिनट और 40 सेकंड का होता है, और इससे भी भारी अपुष्ट आइसोटोप 278Bh का आधा जीवन लगभग 11.5 मिनट का होता है।
द्रव्यमान 260, 261, और 262 वाले सबसे अधिक प्रोटॉन-समृद्ध आइसोटोप सीधे ठंडे संलयन द्वारा उत्पादित किए गए थे, 262 और 264 द्रव्यमान वाले आइसोटोप मीटनेरियम और रोएंटजेनियम की क्षय श्रृंखला में रिपोर्ट किए गए थे, जबकि न्यूट्रॉन-समृद्ध आइसोटोप 265, 266, 267 द्रव्यमान वाले थे। एक्टिनाइड लक्ष्यों के विकिरण में बनाए गए थे। 270, 271, 272, 274, और 278 (अपुष्ट) द्रव्यमान वाले पांच सबसे न्यूट्रॉन-समृद्ध क्रमशः 282Nh, 287Mc, 288Mc, 294Ts, और 290Fl की क्षय श्रृंखला में दिखाई देते हैं। बोहरियम आइसोटोप का आधा जीवन 262mBh के लिए लगभग दस मिलीसेकंड से लेकर 270Bh और 270Bh के लिए लगभग एक मिनट तक होता है, जो अपुष्ट 278Bh के लिए लगभग 11.5 मिनट तक होता है, जो सबसे लंबे समय तक जीवित रहने वाले ज्ञात सुपरहेवी न्यूक्लाइड में से एक है। [23]
अनुमानित गुण
बोहरियम या इसके यौगिकों के बहुत कम गुणों को मापा गया है; यह इसके अत्यधिक सीमित और महंगे उत्पादन के कारण है और यह तथ्य कि बोहरियम (और उसके माता-पिता) बहुत जल्दी सड़ जाते हैं। कुछ विलक्षण रसायन-संबंधी गुणों को मापा गया है, किन्तु बोहरियम धातु के गुण अज्ञात रहते हैं और केवल पूर्वानुमान उपलब्ध हैं।
रासायनिक
बोहरियम संक्रमण धातुओं की 6डी श्रृंखला का पांचवां सदस्य है और मैंगनीज, टेक्नेटियम और रेनियम के नीचे आवर्त सारणी में समूह 7 तत्व का सबसे भारी सदस्य है। समूह के सभी सदस्य सरलता से +7 के अपने समूह ऑक्सीकरण स्तर को चित्रित करते हैं और समूह के उतरते ही स्तर अधिक स्थिर हो जाता है। इस प्रकार बोहरियम से स्थिर +7 अवस्था बनने की उम्मीद है। टेक्नेटियम स्थिर +4 अवस्था भी दिखाता है जबकि रेनियम स्थिर +4 और +3 अवस्थाएँ प्रदर्शित करता है। इसलिए बोहरियम इन निचली अवस्थाओं को भी दिखा सकता है।[6] उच्च +7 ऑक्सीकरण अवस्था ऑक्सीजनों में उपस्थित होने की अधिक संभावना है, जैसे कि परबोह्रेट, BhO−
4, लाइटर परमैंगनेट, परटेक्नेटेट और पेरिनेट के अनुरूप होता है फिर भी, बोहरियम (VII) जलीय घोल में अस्थिर होने की संभावना है, और संभवतः अधिक स्थिर बोहरियम (IV) में सरलता से कम हो जाता है।[2]
टेक्नेटियम और रेनियम को वाष्पशील हेप्टॉक्साइड M2O7 (M = Tc, Re) बनाने के लिए जाना जाता है, इसलिए बोहरियम को भी वाष्पशील ऑक्साइड Bh2O7 बनाना चाहिए। पेरबोह्रिक एसिड, HBhO4 बनाने के लिए ऑक्साइड को पानी में घुलना चाहिए। रेनियम और टेक्नेटियम ऑक्साइड के हैलोजनीकरण से ऑक्सीहैलाइड की एक श्रृंखला बनाते हैं। ऑक्साइड के क्लोरीनीकरण से ऑक्सीक्लोराइड्स MO3Cl बनता है, इसलिए इस प्रतिक्रिया में BhO3Cl2F3 बनना चाहिए। रेनियम यौगिकों ReOF5 और ReF7 के अतिरिक्त भारी तत्वों के लिए फ्लोरिनेशन के परिणामस्वरूप MO3F और MO2F3 उत्पन्न होते हैं। इसलिए, बोरियम के लिए ऑक्सीफ्लोराइड का गठन ईका-रेनियम गुणों को इंगित करने में मदद कर सकता है। [24] चूंकि ऑक्सीक्लोराइड्स असममित हैं, और समूह के नीचे जाने पर उनके बड़े द्विध्रुवीय क्षण होने चाहिए, उन्हें TcO3Cl > ReO3Cl > BhO3Cl क्रम में कम अस्थिर होना चाहिए: इन तीन यौगिकों के सोखने की तापीय धारिता को मापकर 2000 में प्रयोगात्मक रूप से इसकी पुष्टि की गई थी। TcO3Cl और ReO3Cl के मान क्रमशः −51 kJ/mol और −61 kJ/mol हैं; BhO3Cl का प्रायोगिक मान -77.8 kJ/mol है, जो सैद्धांतिक रूप से अपेक्षित मान -78.5 kJ/mol के बहुत निकट है।[2]
भौतिक और परमाणु
बोहरियम के सामान्य परिस्थितियों में ठोस होने की उम्मीद है और हेक्सागोनल क्लोज-पैक क्रिस्टल संरचना (c/a= 1.62), इसके लाइटर कोजेनर (रसायन विज्ञान) रेनियम के समान या [3] फ्रिक के प्रारंभिक अनुमानों में इसका घनत्व 37.1 ग्राम/सेमी अनुमानित किया गया था,[2] किन्तु नई गणना 26–27 g/cm3 के कुछ कम मान का अनुमान लगाती है[4][5]
बोरियम की परमाणु त्रिज्या दोपहर 128 बजे के आसपास होने की उम्मीद है।[2] 7s कक्षक के सापेक्ष स्थिरीकरण और 6d कक्षक के अस्थिर होने के कारण, Bh+ आयन का इलेक्ट्रॉन विन्यास [Rn] 5f14 6d4 7s2 होने की पूर्वानुमान की गई है, जिससे 7s इलेक्ट्रॉन के बजाय 6d इलेक्ट्रॉन निकल जाएगा, जो इसके विपरीत है इसके हल्के समरूप मैंगनीज और टेक्नेटियम का व्यवहार दूसरी ओर, रेनियम, 6s इलेक्ट्रॉन से पहले 5d इलेक्ट्रॉन को छोड़ने में अपने भारी जन्मजात बोरियम का अनुसरण करता है, क्योंकि छठी अवधि तक सापेक्ष प्रभाव महत्वपूर्ण हो गए हैं, जहां वे अन्य चीजों के अतिरिक्त सोने के पीले रंग और कम पिघलने बिंदु का कारण बनते हैं। पारे का. Bh2+ आयन का इलेक्ट्रॉन विन्यास [Rn] 5f14 6d3 7s2 होने की उम्मीद है; इसके विपरीत, Re2+ आयन में [Xe] 4f14 5d5 विन्यास होने की उम्मीद है, इस बार मैंगनीज और टेक्नेटियम के अनुरूप [2] हेक्साकोर्डिनेट हेप्टावेलेंट बोहरियम की आयनिक त्रिज्या 58 pm होने की उम्मीद है (हेप्टावैलेंट मैंगनीज, टेक्नेटियम और रेनियम का मान क्रमशः 46, 57 और 53 pm है)। पेंटावैलेंट बोहरियम की आयनिक त्रिज्या 83 बजे से अधिक होनी चाहिए।[2]
प्रायोगिक रसायन विज्ञान
1995 में, तत्व के अलगाव के प्रयास पर पहली सूची असफल रही थी नए सैद्धांतिक अध्ययनों को यह जांचने के लिए प्रेरित किया कि बोह्रियम की जांच कैसे करें (तुलना के लिए इसके लाइटर होमोलोग्स टेक्नीटियम और रेनियम का उपयोग करके) और अवांछित दूषित तत्वों जैसे कि त्रिसंयोजक एक्टिनाइड, समूह को हटा देंता है। 5 तत्व, और विशेष तत्त्व जिस का प्रभाव रेडियो पर पड़ता है ।[25]
2000 में, यह पुष्टि की गई थी कि यद्यपि सापेक्षतावादी प्रभाव महत्वपूर्ण हैं, बोहरियम विशिष्ट समूह 7 तत्व की तरह व्यवहार करता है।[26] पॉल शेरर संस्थान (पीएसआई) की टीम ने छह परमाणुओं का उपयोग करके रसायन शास्त्र प्रतिक्रिया आयोजित की 267Bh के बीच अभिक्रिया 249BK और 22N में उत्पन्न हुआ था । परिणामी परमाणुओं को तापीयकृत किया गया और hcl/o2 के साथ प्रतिक्रिया की गई वाष्पशील ऑक्सीक्लोराइड बनाने के लिए मिश्रण किया जाता है। प्रतिक्रिया ने इसके लाइटर होमोलॉग्स, टेक्नेटियम (जैसे 108Tc) और रेनियम (as 169Re) इज़ोटेर्मल सोखना घटता को मापा गया और रेनियम ऑक्सीक्लोराइड के समान गुणों वाले वाष्पशील ऑक्सीक्लोराइड के गठन के लिए सशक्त प्रमाण दिए थे। इसने बोहरियम को समूह 7 के विशिष्ट सदस्य के रूप में रखा गया था।[27] इस प्रयोग में टेक्नेटियम, रेनियम और बोहरियम के ऑक्सीक्लोराइड्स के सोखने की एन्थैल्पी को मापा गया था, जो सैद्धांतिक पूर्वानुमानो के साथ बहुत अच्छी तरह से सहमत हैं और TcO3Cl > ReO3Cl > BhO3Cl के समूह 7 में ऑक्सीक्लोराइड की अस्थिरता को कम करने के क्रम को प्रयुक्त करते हैं।[2]
- 2 Bh + 3 O
2 + 2 HCl → 2 BhO
3Cl + H
2
बोहरियम के लंबे समय तक जीवित रहने वाले भारी आइसोटोप, भारी तत्वों की डाटर्स के रूप में उत्पादित होते हैं, जो भविष्य के रेडियोकेमिकल प्रयोगों के लिए लाभ प्रदान करते हैं। यद्यपि भारी आइसोटोप 274बीएच को इसके उत्पादन के लिए एक दुर्लभ और अत्यधिक रेडियोधर्मी बर्केलियम लक्ष्य की आवश्यकता होती है, आइसोटोप 272Bh, 271Bh, और 270Bh को अधिक सरलता से उत्पादित मोस्कोवियम और निहोनियम आइसोटोप की डाटर्स के रूप में सरलता से उत्पादित किया जा सकता है।[28]
टिप्पणियाँ
संदर्भ
- ↑ Johnson, E.; Fricke, B.; Jacob, T.; Dong, C. Z.; Fritzsche, S.; Pershina, V. (2002). "Ionization potentials and radii of neutral and ionized species of elements 107 (bohrium) and 108 (hassium) from extended multiconfiguration Dirac–Fock calculations". The Journal of Chemical Physics. 116 (5): 1862–1868. Bibcode:2002JChPh.116.1862J. doi:10.1063/1.1430256.
- ↑ 2.00 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 Hoffman, Darleane C.; Lee, Diana M.; Pershina, Valeria (2006). "Transactinides and the future elements". In Morss; Edelstein, Norman M.; Fuger, Jean (eds.). The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Dordrecht, The Netherlands: Springer Science+Business Media. ISBN 1-4020-3555-1.
- ↑ 3.0 3.1 3.2 Östlin, A.; Vitos, L. (2011). "First-principles calculation of the structural stability of 6d transition metals". Physical Review B. 84 (11). Bibcode:2011PhRvB..84k3104O. doi:10.1103/PhysRevB.84.113104.
- ↑ 4.0 4.1 Gyanchandani, Jyoti; Sikka, S. K. (10 May 2011). "Physical properties of the 6 d -series elements from density functional theory: Close similarity to lighter transition metals". Physical Review B. 83 (17): 172101. doi:10.1103/PhysRevB.83.172101.
- ↑ 5.0 5.1 Kratz; Lieser (2013). Nuclear and Radiochemistry: Fundamentals and Applications (3rd ed.). p. 631.
- ↑ 6.0 6.1 Fricke, Burkhard (1975). "Superheavy elements: a prediction of their chemical and physical properties". Recent Impact of Physics on Inorganic Chemistry. Structure and Bonding. 21: 89–144. doi:10.1007/BFb0116498. ISBN 978-3-540-07109-9. Retrieved 4 October 2013.
- ↑ Chemical Data. Bohrium - Bh, Royal Chemical Society
- ↑ Yu; Demin, A.G.; Danilov, N.A.; Flerov, G.N.; Ivanov, M.P.; Iljinov, A.S.; Kolesnikov, N.N.; Markov, B.N.; Plotko, V.M.; Tretyakova, S.P. (1976). "तत्वों के न्यूट्रॉन की कमी वाले समस्थानिकों के सहज विखंडन पर". Nuclear Physics A. 273: 505–522. doi:10.1016/0375-9474(76)90607-2.
- ↑ 9.0 9.1 Barber, R. C.; Greenwood, N. N.; Hrynkiewicz, A. Z.; Jeannin, Y. P.; Lefort, M.; Sakai, M.; Ulehla, I.; Wapstra, A. P.; Wilkinson, D. H. (1993). "Discovery of the transfermium elements. Part II: Introduction to discovery profiles. Part III: Discovery profiles of the transfermium elements". Pure and Applied Chemistry. 65 (8): 1757. doi:10.1351/pac199365081757. S2CID 195819585.
- ↑ 10.0 10.1 10.2 Münzenberg, G.; Hofmann, S.; Heßberger, F. P.; Reisdorf, W.; Schmidt, K. H.; Schneider, J. H. R.; Armbruster, P.; Sahm, C. C.; Thuma, B. (1981). "Identification of element 107 by α correlation chains". Zeitschrift für Physik A. 300 (1): 107–8. Bibcode:1981ZPhyA.300..107M. doi:10.1007/BF01412623. S2CID 118312056. Retrieved 24 December 2016.
- ↑ Ghiorso, A.; Seaborg, G. T.; Organessian, Yu. Ts.; Zvara, I.; Armbruster, P.; Hessberger, F. P.; Hofmann, S.; Leino, M.; Munzenberg, G.; Reisdorf, W.; Schmidt, K.-H. (1993). "Responses on 'Discovery of the transfermium elements' by Lawrence Berkeley Laboratory, California; Joint Institute for Nuclear Research, Dubna; and Gesellschaft fur Schwerionenforschung, Darmstadt followed by reply to responses by the Transfermium Working Group". Pure and Applied Chemistry. 65 (8): 1815–1824. doi:10.1351/pac199365081815.
- ↑ "Names and symbols of transfermium elements (IUPAC Recommendations 1994)". Pure and Applied Chemistry. 66 (12): 2419–2421. 1994. doi:10.1351/pac199466122419.
- ↑ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. pp. 337–9. Electronic version.
- ↑ 14.0 14.1 14.2 Sonzogni, Alejandro. "Interactive Chart of Nuclides". National Nuclear Data Center: Brookhaven National Laboratory. Retrieved 2008-06-06.
- ↑ 15.0 15.1 Gray, Theodore (2002–2010). "The Photographic Periodic Table of the Elements". periodictable.com. Retrieved 16 November 2012.
- ↑ Nelson, S.; Gregorich, K.; Dragojević, I.; Garcia, M.; Gates, J.; Sudowe, R.; Nitsche, H. (2008). "Lightest Isotope of Bh Produced via the Bi209(Cr52,n)Bh260 Reaction" (PDF). Physical Review Letters. 100 (2): 022501. Bibcode:2008PhRvL.100b2501N. doi:10.1103/PhysRevLett.100.022501. PMID 18232860. S2CID 1242390. Archived (PDF) from the original on 2022-10-09.
- ↑ Münzenberg, G.; Armbruster, P.; Hofmann, S.; Heßberger, F. P.; Folger, H.; Keller, J. G.; Ninov, V.; Poppensieker, K.; et al. (1989). "Element 107". Zeitschrift für Physik A. 333 (2): 163. Bibcode:1989ZPhyA.333..163M. doi:10.1007/BF01565147. S2CID 186231905.
- ↑ Hofmann, S.; Ninov, V.; Heßberger, F. P.; Armbruster, P.; Folger, H.; Münzenberg, G.; Schött, H. J.; Popeko, A. G.; Yeremin, A. V.; Andreyev, A. N.; Saro, S.; Janik, R.; Leino, M. (1995). "The new element 111". Zeitschrift für Physik A. 350 (4): 281. Bibcode:1995ZPhyA.350..281H. doi:10.1007/BF01291182. S2CID 18804192.
- ↑ Gan, Z.G.; Guo, J. S.; Wu, X. L.; Qin, Z.; Fan, H. M.; Lei, X. G.; Liu, H. Y.; Guo, B.; et al. (2004). "New isotope 265Bh". The European Physical Journal A. 20 (3): 385. Bibcode:2004EPJA...20..385G. doi:10.1140/epja/i2004-10020-2. S2CID 120622108.
- ↑ 20.0 20.1 Wilk, P. A.; Gregorich, K. E.; Turler, A.; Laue, C. A.; Eichler, R.; Ninov V, V.; Adams, J. L.; Kirbach, U. W.; et al. (2000). "Evidence for New Isotopes of Element 107: 266Bh and 267Bh". Physical Review Letters. 85 (13): 2697–700. Bibcode:2000PhRvL..85.2697W. doi:10.1103/PhysRevLett.85.2697. PMID 10991211.
- ↑ 21.0 21.1 21.2 Oganessian, Yu. Ts.; Utyonkov, V. K.; Kovrizhnykh, N. D.; et al. (2022). "New isotope 286Mc produced in the 243Am+48Ca reaction". Physical Review C. 106 (64306): 064306. Bibcode:2022PhRvC.106f4306O. doi:10.1103/PhysRevC.106.064306. S2CID 254435744.
- ↑ 22.0 22.1 22.2 Oganessian, Yu. Ts. (2007). "Heaviest Nuclei Produced in 48Ca-induced Reactions (Synthesis and Decay Properties)". In Penionzhkevich, Yu. E.; Cherepanov, E. A. (eds.). AIP Conference Proceedings: International Symposium on Exotic Nuclei. Vol. 912. p. 235. doi:10.1063/1.2746600. ISBN 978-0-7354-0420-5.
- ↑ Münzenberg, G.; Gupta, M. (2011). "Production and Identification of Transactinide Elements". In Vértes, Attila; Nagy, Sándor; Klencsár, Zoltán; Lovas, Rezső G.; Rösch, Frank (eds.). हैंडबुक ऑफ न्यूक्लियर केमिस्ट्री: प्रोडक्शन एंड आइडेंटिफिकेशन ऑफ ट्रांसएक्टिनाइड एलिमेंट्स. p. 877. doi:10.1007/978-1-4419-0720-2_19. ISBN 978-1-4419-0719-6.
- ↑ Hans Georg Nadler "Rhenium and Rhenium Compounds" Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2000. doi:10.1002/14356007.a23_199
- ↑ Malmbeck, R.; Skarnemark, G.; Alstad, J.; Fure, K.; Johansson, M.; Omtvedt, J. P. (2000). "बोहरियम के अध्ययन के लिए प्रस्तावित रासायनिक पृथक्करण प्रक्रिया". Journal of Radioanalytical and Nuclear Chemistry. 246 (2): 349. doi:10.1023/A:1006791027906. S2CID 93640208.
- ↑ Gäggeler, H. W.; Eichler, R.; Brüchle, W.; Dressler, R.; Düllmann, Ch. E.; Eichler, B.; Gregorich, K. E.; Hoffman, D. C.; et al. (2000). "Chemical characterization of bohrium (element 107)". Nature. 407 (6800): 63–5. Bibcode:2000Natur.407...63E. doi:10.1038/35024044. PMID 10993071. S2CID 4398253.
- ↑ Eichler, R.; et al. "Gas chemical investigation of bohrium (Bh, element 107)" (PDF). GSI Annual Report 2000. Archived from the original (PDF) on 2012-02-19. Retrieved 2008-02-29.
- ↑ Moody, Ken (2013-11-30). "Synthesis of Superheavy Elements". In Schädel, Matthias; Shaughnessy, Dawn (eds.). अतिभारी तत्वों का रसायन (2nd ed.). Springer Science & Business Media. pp. 24–8. ISBN 9783642374661.
ग्रन्थसूची
- Audi, G.; Kondev, F. G.; Wang, M.; et al. (2017). "The NUBASE2016 evaluation of nuclear properties". Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- Beiser, A. (2003). Concepts of modern physics (6th ed.). McGraw-Hill. ISBN 978-0-07-244848-1. OCLC 48965418.
- Hoffman, D. C.; Ghiorso, A.; Seaborg, G. T. (2000). The Transuranium People: The Inside Story. World Scientific. ISBN 978-1-78-326244-1.
- Kragh, H. (2018). From Transuranic to Superheavy Elements: A Story of Dispute and Creation. Springer. ISBN 978-3-319-75813-8.
- Zagrebaev, V.; Karpov, A.; Greiner, W. (2013). "Future of superheavy element research: Which nuclei could be synthesized within the next few years?". Journal of Physics: Conference Series. 420 (1): 012001. arXiv:1207.5700. Bibcode:2013JPhCS.420a2001Z. doi:10.1088/1742-6596/420/1/012001. ISSN 1742-6588. S2CID 55434734.
बाहरी संबंध
 Media related to बोरियम at Wikimedia Commons
Media related to बोरियम at Wikimedia Commons- Bohrium at The Periodic Table of Videos (University of Nottingham)
- Templates that generate short descriptions
- Articles with hAudio microformats
- Pages including recorded pronunciations
- Pages using infobox element with unknown parameters
- Collapse templates
- Navigational boxes
- Navigational boxes without horizontal lists
- Sidebars with styles needing conversion
- Templates generating microformats
- Templates that are not mobile friendly
- Wikipedia metatemplates
- Created On 23/05/2023
- Machine Translated Page
- Vigyan Ready